2024年医疗器械FDA注册费用是多少?

2023年7月28日,FDA通过联邦公告 (Federal Reister )公布了2023财政年医疗器械注册收费标准,即,Medical Device User Fee,该费用于2023年10月1日开始实施,至2024年9月30日
企业年费较2023年的USD 6,493大幅度上涨,为USD 7,653。FDA 510(k)标准收费从2023年的19870美金上涨到21760美金;小微企业收费从2023年的4967美金上涨到5440美金。
自2008年以来美国FDA开始收取医疗器械年费逐年增长,从2008年的USD1,706一直涨到2024年的USD7653。为数不少的低附加值中小型出口医疗器械企业生存压力日益增大。上海世复检测为您列明医疗器械FDA注册历年年费收费标准的增长趋势图:
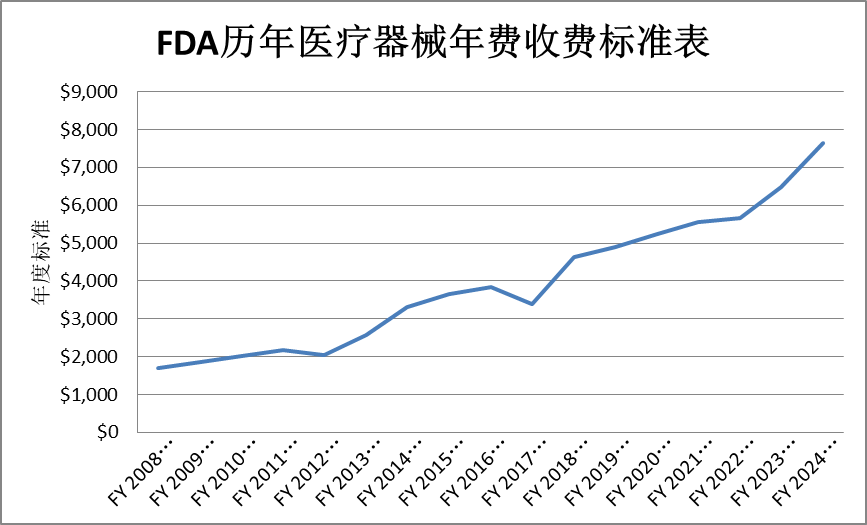
FDA注册的财政年为每年的10月1日起,计算一年。因此,上海世复检测将从10月1日起为中国用户提供FDA医疗器械注册更新服务。
2023年7月28日公布了2024财年(2023年10月1日 – 2024年9月30日)的FDA各项服务的收费案。
Important Information on Medical Device User Fees for Fiscal Year 2024
(适用于FDA 2024财年:2023年10月1日至2024年9月30日)
主要费率:
项目 | 2024财年(2023.10.01-2024.09.30) |
2024财年医疗器械公司注册年度认证费 | USD 7,653/个制造商 |
2024财年FDA510(K)审核费(每个510K申请) | USD21,760/个申请 USD5,440/个申请(小规模企业) |
*FDA 将小型企业定义为总收入或销售额不超过 1 亿美元的企业,包括来自其附属公司的收入或销售额。此外,如果小型企业的总收入或销售额为 3000 万美元或以下,则有资格免除其首次 PMA、PDP、PMR 或 BLA 的费用。
其他费率:
FY2024 User Fees for Medical Device Submissions
2024财年医疗器械提交的用户费用
Application Type | Standard Fee(2023) | Standard Fee(2024) | Small Business Fee†(2023) | Small Business Fee†(2024) |
510(k) | $19,870 | $21,760 | $4,967 | $5,440 |
513(g) | $5,961 | $6,528 | $2,980 | $3,264 |
PMA, PDP, PMR, BLA | $441,547 | $483,560 | $110,387 | $120,890 |
De Novo Classification Request | $132,464 | $145,068 | $33,116 | $36,267 |
Panel-track Supplement | $353,238 | $386,848 | $88,309 | $96,712 |
180-Day Supplement | $66,232 | $72,534 | $16,558 | $18,134 |
Real-Time Supplement | $30,908 | $33,849 | $7,727 | $8,462 |
BLA Efficacy Supplement | $441,547 | $483,560 | $110,387 | $120,890 |
30-Day Notice | $7,065 | $7,737 | $3,532 | $3,869 |
Annual Fee for Periodic Reporting on a Class III device (PMAs,PDPs) | $15,454 | $16,925 | $3,864 | $4,231 |
了解更多关于医疗器械FDA注册,欢迎来电咨询世复检测 021-65667889/13386062867。
最新动态
- 上海世复检测电话号码变更通知 2022-06-17 00:00:00
- RoHS 2.0(10项)鼠标均质材料铅、镉、汞实验室拆解检测 2026-05-09 15:41:52
- REACH邻苯(6P/7P):婴儿咬咬乐硅胶与塑料手柄的安全性验证 2026-05-09 15:40:17
- CE玩具指令(EN 62115):儿童智能早教机的电安全与外壳阻燃验证 2026-05-09 15:38:36
- CE RED (EN 300 328):无线智能水表在2.4GHz频段的自适应性与发射功率合规指南 2026-05-09 15:36:45
- 基于IEC 61000-4-5标准的家用智能控制插座浪涌抗扰度分析 2026-05-09 15:34:42
- 欧盟CE LVD 2014/35/EU:低电压电气产品的安全准入基石 2026-05-09 15:32:38
- FCC ID认证实务:2.4G无线领夹麦克风Part 15C发射功率测试全解 2026-05-09 15:07:53
- 智能喂宠机的CE RED合规之路:EN 300 328标准下的无线射频测试全解 2026-05-09 15:04:22
- 暖碗机闯俄关:EAC TR CU 004/2011认证全攻略 2026-05-09 15:02:20
